°°°°Īĺ—–ĺŅ ◊īőįl¨FŃňŌ¬«ūńX “Ň‘ļňļÕ “Ň‘Ō¬ļňīś‘ŕīőēÉ“Ļ…ķőÔĻ̬…£¨Ĺ“ ĺŃňīőēÉ“ĻĻ̬…Ķńģa…ķőĽŁcļÕ…ŮĹõĺWĹjôC÷∆°£—–ĺŅĹYĻŻĆ¶ņŪĹ‚Ą”őÔňĮ√Ŗ÷‹∆ŕ°Ęůwúō’{ĻĚļÕľ§ňō∑÷√ŕĶ»––일ÚĻ¶ń‹ĶńīőēÉ“ĻĻ̬…ĺŖ”–÷ō“™ÜĘ ĺ£¨Ņ…ń‹ěťť_įl…ķőÔĻ̬…ģź≥£ļÕňĮ√Ŗ’ŌĶKĶń–¬Įü∑®ŐŠĻ©–¬ňľ¬∑°£
°°°°ďĢŃňĹ‚£¨Ņō÷∆ēÉ“ĻĻ̬…ÍPśIĽý“ÚĶńįl¨Fę@Ķ√Ńň2017ńÍ÷Zōź†Ė…ķņŪĆWĽÚŠtĆW™Ą°£…ķőÔĻ̬…‘॔÷≤őÔ÷–ŹV∑ļīś‘ŕ£¨◊Ó≥£“äĶń «÷‹∆ŕěť24–°ērĶńēÉ“ĻĻ̬…£¨»ňÓźĶńňĮ√Ŗ-”X–—÷‹∆ŕ∑ŻļŌĶš–ÕĶń…ķőÔĻ̬…°£»Ľ∂Ý£¨≤ł»ťĄ”őÔĶńń≥–©––일ÚĻ¶ń‹ŖÄĪŪ¨F≥Ų÷‹∆ŕ∂Ő”ŕ24–°ērĶńīőēÉ“ĻĻ̬…£¨»Á»ňÓź“ĻťgĶńŅžĄ”—Ř-∑«ŅžĄ”—ŘňĮ√Ŗ—≠≠h°ĘŌ¬«ūńXÉ»ľ§ňō∑÷√ŕļÕůwúō’{ĻĚĶ»°£”…”ŕīőēÉ“ĻĻ̬…ļÕēÉ“ĻĻ̬…Ĺõ≥£įťŽS‘ŕ“Ľ∆ū£¨ ĻīőēÉ“ĻĻ̬…Ķń—–ĺŅĺŖ”–Žy∂»°£“Úīň£¨Ĺ“ ĺīőēÉ“ĻĻ̬…Ķńįl…ķôC÷∆ «÷ō“™ĶńŅ∆ĆWÜĖÓ}°£
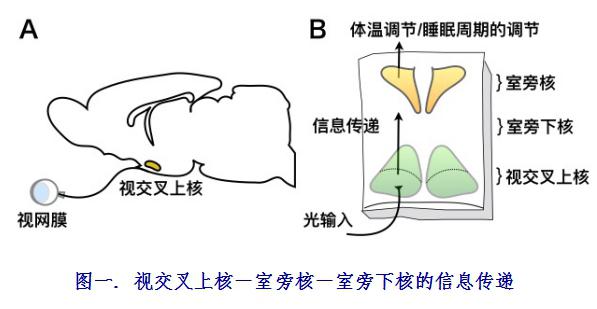
°°°°ěťŐĹňųīőēÉ“ĻĻ̬…Ķńįl…ķôC÷∆£¨—–ĺŅ»ňÜT‘ŕ–¬…ķ4-6Őž–° ůĶńńX«–∆¨…ŌĪŪŖ_‚}Žx◊”÷ł 奩GCaMP6sĶįį◊£¨‘ďĶįį◊Ņ…“‘ĪĽľ§įlģa…ķü…Ļ‚≤ĘŽSľöįŻÉ»‚}Žx◊”ĶńĄ”ĎB◊ÉĽĮ∂Ýįl…ķŹä∂»◊ÉĽĮ£¨‚}–ŇŐĖĶńŹä»ű∑ī”≥…ŮĹõ‘™ĶńĽÓĄ”∂»°£ņŻ”√Ććērü…Ļ‚≥…ŌŮľľ–g£®Time-lapse imaging£©ŖBņm“Ľ÷‹“‘…ŌĪOúyŽxůwńX∆¨÷–…ŮĹõ‘™‚}Žx◊”Ě‚∂»Ķń◊ÉĽĮ£¨įl¨F‘ŕŌ¬«ūńX “Ň‘ļň£®PVN£©°Ę “Ň‘Ō¬ļň£®SPZ£©Ö^”ÚļÕ“Ľ≤Ņ∑÷“ēĹĽ≤ś…Ōļň£®SCN£©Ö^”Ú£¨īś‘ŕ÷‹∆ŕěť0.5°ę4–°ērĶńīőēÉ“ĻĻ̬…°£Ŗ@∑NīőēÉ“ĻĻ̬…ŹńSPZ-PVNÖ^”Úģa…ķ£¨īőēÉ“ĻĻ̬…–ŇŐĖŅ…“‘∑īūĀĶĹēÉ“ĻĻ̬…÷–ė–SCN£®ąD“Ľ£©°£Õ®Ŗ^ňéņŪĆW ÷∂ő£¨ŖM“Ľ≤Ĺįl¨FĻ»įĪňŠń‹ŌĶĹyÖĘŇcŃňīőēÉ“ĻĻ̬…Ķń–ő≥…£¨‚cŽx◊”Õ®Ķņ◊ŤĒŗĄ©TTX√Űł–Ķń…ŮĹõĺWĹjÖĘŇcīőēÉ“Ļ‚}Ļ̬…ĶńÕ¨≤ĹĽĮ°£
°°°°ŹÕĶ©īůĆW≤© Ņ…ķÖ«Ť§ÁŪļÕĪĪļ£ĶņīůĆWė\ńĺŃŃĹťłĪĹŐ ŕěťĪĺőńĶńĻ≤Õ¨Ķŕ“Ľ◊ų’Ŗ£¨ŹÕĶ©īůĆWŁS÷ĺѶĹŐ ŕļÕĪĪļ£ĶņīůĆWė\ńĺŃŃĹťłĪĹŐ ŕěťĪĺőńĶńĻ≤Õ¨Õ®”ć◊ų’Ŗ£¨ŹÕĶ©īůĆWěťĶŕ“Ľ◊ų’ŖÜőőĽ°£‘ď—–ĺŅĶ√ĶĹŃňáÝľ“◊‘»ĽŅ∆ĆWĽýĹū÷ōŁcŪóńŅĶ»ĽýĹūĶńŔY÷ķ°£
°°°°





 °įĺŇ°§“Ľįň°Ī ¬◊ÉĪ¨įl87÷‹ńÍ Ŗ|Ćé…ÚÍĖ Ňe––°įőūÕŁĺŇ°§“Ľįň°Ī◊≤ÁäÝQĺĮÉx Ĺ
°įĺŇ°§“Ľįň°Ī ¬◊ÉĪ¨įl87÷‹ńÍ Ŗ|Ćé…ÚÍĖ Ňe––°įőūÕŁĺŇ°§“Ľįň°Ī◊≤ÁäÝQĺĮÉx Ĺ
